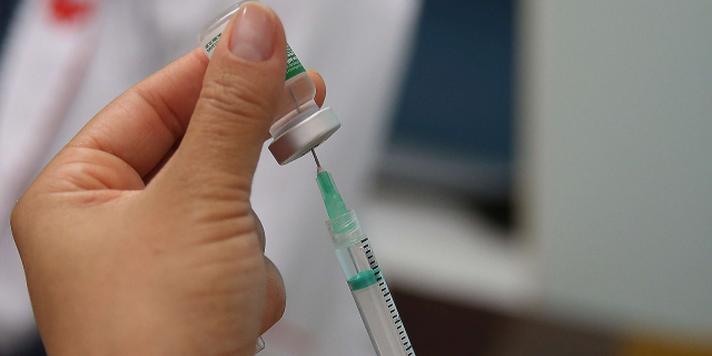
O Hospital das Clínicas de Belo Horizonte é um dos 20 centros de pesquisa brasileiros escolhidos para atuar no estudo da vacina contra o novo coronavírus desenvolvida pela Janssen-Cilag, divisão farmacêutica da empresa norte-americana Johnson-Johnson, mas o início do trabalho em Minas depende da aprovação da comissão de ética da UFMG.
Para que a pesquisa em voluntários possa ser realizada no Brasil, a candidata a vacina precisa ser aprovada pelo Conselho Nacional de Ética em Pesquisa (Conep), órgão do Ministério da Saúde, e de cada uma das comissões de ética dos centros participantes. Os testes já foram autorizados pela Agência Nacional de Vigilância Sanitária (Anvisa) e a Santa Casa de BH também participará do estudo.
Em Belo Horizonte, a pesquisa na UFMG sobre a vacina Ad26.COV2.S ficará a cargo do professor Jorge Andrade Pinto, que é chefe do Serviço de Imunologia do Hospital das Clínicas (HC) da UFMG e consultor da Organização Mundial da Saúde. A expectativa é que a aprovação pelo Conep aconteça ainda esta semana e os estudos possam ser iniciados em setembro.
O ensaio clínico aprovado pela Anvisa está na fase 3 e deverá ser randomizado e controlado por placebo, ou seja, metade dos voluntários receberão uma dose de Ad26.COV2.S, enquanto o outro grupo receberá uma substância neutra. Voluntários e médicos não poderão saber quem recebeu a vacina ou quem tomou o placebo (duplo cego). Ainda não foi divulgado qual será o perfil do grupo voluntário, mas estima-se que 7 mil pessoas serão convocadas para participação do estudo.
Quarta vacina no Brasil
Esta é a quarta vacina a receber aprovação pela Anvisa para ser testada no Brasil. No dia 2 de junho, a Agência autorizou o ensaio clínico da vacina desenvolvida pela Universidade de Oxford, no Reino Unido; em 3 de julho, o da vacina desenvolvida pela empresa Sinovac Research & Development Co. Ltd., em parceria com o Instituto Butantan; e em 21 de julho, a desenvolvida pela BioNTech e Wyeth/Pfizer.
A vacina chinesa Coronavac, da Sinovac, está na fase 3 de testes e voluntários mineiros participam dos estudos, todos profissionais de saúde que atuam na linha de frente de atendimento a pacientes com Covid. Em Belo Horizonte, os testes são coordenados pelo pesquisador Mauro Teixeira Martins, coordenador do Centro de Pesquisa e Desenvolvimento de Fármacos do Instituto de Ciências Biológicas (ICB), da UFMG.
Vacina nos EUA
No início de agosto, a Johnson & Johnson anunciou um acordo com o governo dos Estados Unidos para a fabricação e entrega doméstica em grande escala de 100 milhões de doses da vacina experimental Ad26.COV2.S, para uso no país após a aprovação ou autorização de uso de emergência pela US Food and Drug Administration (FDA), órgão equivalente à Anvisa.
O acordo gira em torno de US$ 1 bilhão. O governo dos EUA também se comprometeu a comprar 200 milhões de doses adicionais de Ad26.COV2.S sob um contrato subsequente.
"A empresa está avaliando os regimes de uma e duas doses em seu programa clínico e trabalhando diligentemente para garantir um acesso amplo e global à vacina após a aprovação ou autorização dos reguladores. A Johnson & Johnson pretende cumprir sua meta de fornecer mais de um bilhão de doses globalmente ao longo de 2021, desde que a vacina seja segura e eficaz", diz a empresa farmacêutica em seu site brasileiro.