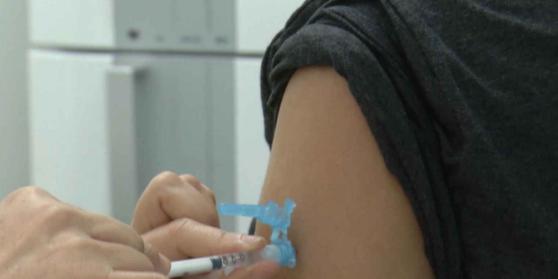
A farmacêutica norte-americana Pfizer afirmou, nesta sexta-feira (20), que planeja pedir aos órgãos reguladores de saúde dos Estados Unidos a aprovação para uso emergencial da vacina desenvolvida em parceria com a BioNTech contra a Covid-19.
Para que o imunizante chegue à população, a Food and Drug Administration (Administração de Alimentos e Medicamentos) deverá constatar se ele oferece segurança e resultados satisfatórios.
Ao obter o registro junto à FDA, vem a fase de logística. As companhias planejam começar a distribuição das doses até o fim do próximo mês.
No entanto, ainda não há prazo para uma resposta da agência reguladora. Nesta semana, um grupo de pesquisadores informou que a vacina, aplicada em duas doses, obteve 95% de eficiência em produzir resposta imunológica nos pacientes.
Vacinação no Brasil
Na última terça-feira (17), o Ministério da Saúde se reuniu com uma equipe da Pfizer para que os representantes do laboratório apresentassem o andamento da pesquisa e para que fossem avaliadas as condições de compra, logística e armazenamento. Outras companhias também serão procuradas, com a farmacêutica estadunidense Moderna, o consórcio russo responsável pela Sputinik V, a Janssen (braço da Johnson e Johnson), e equipe da Covaxin, da Índia.
Leia mais: